2.3 Antibiotische Resistenztestung
Die Untersuchung der antibiotischen Empfindlichkeit von Krankheitserregern stellt eine Kernaufgabe des mikrobiologisch-diagnostischen Labors dar. Ziel ist eine möglichst genaue Bestimmung („Antibiogramm“), die darüber Aufschluss gibt, mit welchen Antibiotika ein Therapieerfolg wahrscheinlich ist. Eine Resistenzprüfung wird bei allen pathogenen Bakterien durchgeführt, welche eine nicht vorhersehbare antibiotische Empfindlichkeit aufweisen; z. B. wird bei beta-hämolytischen Streptokokken keine Resistenzprüfung für Penicillin G durchgeführt, da bisher keine Penicillin G - resistenten Stämme beschrieben wurden. Andere Erreger, wie z. B. Escherichia coli, können jedoch eine Vielzahl von Resistenzmechanismen aufweisen.
Die Auswahl der getesteten Antibiotika wird den Substanzen angepasst, welche von der Mehrzahl der Auftraggeber verwendet werden. Wir verzichten auf die Angabe von Markennamen. Diese können Sie im «Arzneimittel-Kompendium der Schweiz» finden. Für Informationen zu Resistenzprüfungen von speziellen Erregern siehe auch Kapitel 6 (Mykobakteriologie / Tuberkulose) und Kapitel 3 (Mykologie).
Ausgangsmaterial für Resistenzprüfungen sind Reinkulturen von Erregern, die aus Patientenproben isoliert oder von externen Laboratorien eingesandt wurden. Zur Bestimmung der Antibiotikaempfindlichkeit eines Pathogens kommen hauptsächlich zwei Verfahren zum Einsatz:
Disk-Diffusionsmethode („Kirby-Bauer Test“)
Die Disk-Diffusionsmethode stellt am IMM die Standardmethode der antibiotischen Resistenzprüfung dar. Antibiotikahaltige Blättchen werden auf eine Agarplatte aufgelegt, welche zuvor mit dem zu testenden Bakterienstamm beimpft wurde. Das Antibiotikum diffundiert radial in den Agar (Abb. 1) und formt dabei einen ringförmigen Konzentrationsgradienten. Während der Bebrütung wachsen die Bakterien zu einem „Rasen“ zusammen und es formen sich entsprechend der antibiotischen Empfindlichkeit kreisförmige Zonen um die Antibiotikablättchen. Vorteile der Disk-Diffusionsmethode sind ihre Flexibilität bei der Antibiotikaauswahl sowie die Möglichkeit, neben den Hemmzonen eine Vielzahl weiterer Informationen zu gewinnen. Das IMM treibt die Weiterentwicklung und Verbesserung der Disk-Diffusionstestung in den Einheiten „Antibiotic Resistance Unit“ und „Laboratory Automation Unit“ mit grossem Einsatz aktiv voran.
Minimale Hemmkonzentrationen (MHK)
Die Minimale Hemmkonzentration beschreibt die antibiotische Empfindlichkeit in Konzentrationseinheiten von Milligramm Antibiotikum pro Liter (mg/L). Damit wird ein direkter Vergleich mit erreichbaren Serumkonzentrationen des jeweiligen Wirkstoffes möglich. Die Minimale Hemmkonzentration liegt bei der niedrigsten Antibiotikakonzentration vor, bei der kein Erregerwachstum nachgewiesen werden kann (Abb. 2a). Zur Bestimmung der MHK wird am IMM meist die international akzeptierte Gradientendiffusion eingesetzt, bei der ein mit einem Antibiotikagradienten imprägnierter Kunststoffstreifen auf eine mit dem Erreger beimpfte Agarplatte aufgebracht wird (E-Test, Abb. 2b).
Methodisch ist die Bestimmung der MHK nicht genauer als die Disk-Diffusionsmethode. MHK-Bestimmungen werden auf gezielte Anfrage hin durchgeführt. Neben der Interpretation der Ergebnisse werden die MHK-Grenzwerte, die klinische Empfindlichkeit und Resistenz angeben, mitgeteilt.
Nach Abschluss der bakteriologischen Untersuchung werden die isolierten Erreger verworfen; es muss also dem Bakteriologielabor rechtzeitig mitgeteilt werden, ob gegebenenfalls MHKs durchgeführt werden sollen. Eine Ausnahme bilden die aus Blutkulturen isolierten Erreger, die drei Monate lang aufbewahrt werden.
Ergebnisse der MHK Bestimmung sind innerhalb von 24 bis 72 Stunden zu erwarten.
Interpretation von Resistenzprüfungen
Die Klassifizierung der antibiotischen Resistenz erfolgt traditionell in drei „klinische“ Kategorien: „Sensibel (S)“, d. h. eine hohe Wahrscheinlichkeit für eine erfolgreiche Therapie; „Intermediär (I)“, d. h. eine unsichere Wahrscheinlichkeit für eine erfolgreiche Therapie; „Resistent (R)“, d. h. eine geringe Wahrscheinlichkeit für eine erfolgreiche Therapie. Zur Klassifizierung werden in der Regel die jeweils neuesten Empfehlungen des "European Committee for Antimicrobial Susceptibility Testing" (EUCAST) herangezogen. Ergänzend werden Richtlinien des "Clinical and Laboratory Standards Institute" (CLSI), verfügbare Literatur, sowie am IMM gewonnene Erkenntnisse berücksichtigt (Antibiotic Resistance Unit, eigene Forschung).
Neben der Einteilung der Empfindlichkeit in die Kategorien S, I, und R kommen Interpretationsregeln zum Einsatz, die unter anderem die natürliche Empfindlichkeit von Bakterienspezies berücksichtigen oder die Kategorisierung im Hinblick auf spezielle Resistenzmechanismen modifizieren. Es werden beispielsweise Markersubstanzen eingesetzt, welche sehr empfindlich Resistenzmechanismen nachweisen, die zu einem Therapieversagen führen können. So werden z. B. Staphylokokkenstämme, welche für Clindamycin in vitro sensibel erscheinen, bei denen jedoch der induzierbare MLS-Resistenzmechanismus (Abb. 3) nachgewiesen werden konnte, als Clindamycin resistent berichtet, da unter Therapie mit Clindamycin eine rasche Resistenzentwicklung vorhersehbar ist. Des Weiteren beschränkt sich das Ergebnis der Prüfung einer bestimmten Substanz meist nicht nur auf diese selbst, sondern erstreckt sich auf eine ganze Klasse von Antibiotika, für welche die untersuchte Substanz als repräsentativ ausgewählt wurde.
Bei der Interpretation der Daten muss berücksichtigt werden, dass die Ergebnisse aufgrund von technischer und biologischer Variabilität variieren können, z. B. bei der Bestimmung der Minimalen Hemmkonzentration (MHK, s. o.) um ±1 Verdünnungsstufe, bei der Disk-Diffusionmethode um +/- 2-3 mm. Bei der antibiotischen Empfindlichkeitsprüfung ein- und desselben Erregerstammes aus verschiedenen Patientenproben kann diese Variabilität unter Umständen zu abweichenden Interpretationen im Antibiogramm führen.
Bestimmung von speziellen Resistenzmechanismen
Bestimmte Resistenzmechanismen, insbesondere jene, die zu Multiresistenz („Multi Drug Resistance“ - MDR) führen, sind von spitalhygienischer Bedeutung. Zu diesen Mechanismen zählen z. B. die Methicillin-Resistenz bei Staphylococcus aureus („MRSA“), die Vancomycin-Resistenz bei Enterokokken, bei Gram-negativen Mikroorganismen die Extended-Spektrum Beta-Laktamasen (ESBL), die AmpC-Betalaktamasen oder die Carbapenemasen.
Die genannten Mechanismen werden am IMM aktiv durch Screening gesucht und mittels standardisierter und vom IMM eigens entwickelter diagnostischer Algorithmen nachgewiesen. Das Vorhandensein dieser Mechanismen wird auf den Laborberichten vermerkt und an die Spitalhygiene weitergeleitet.
Abbildungen
Abb. 1: Prinzip und Beispiel der Disk-Diffusionsmethode
Abb. 2: Prinzip der Minimalen Hemmkonzentration
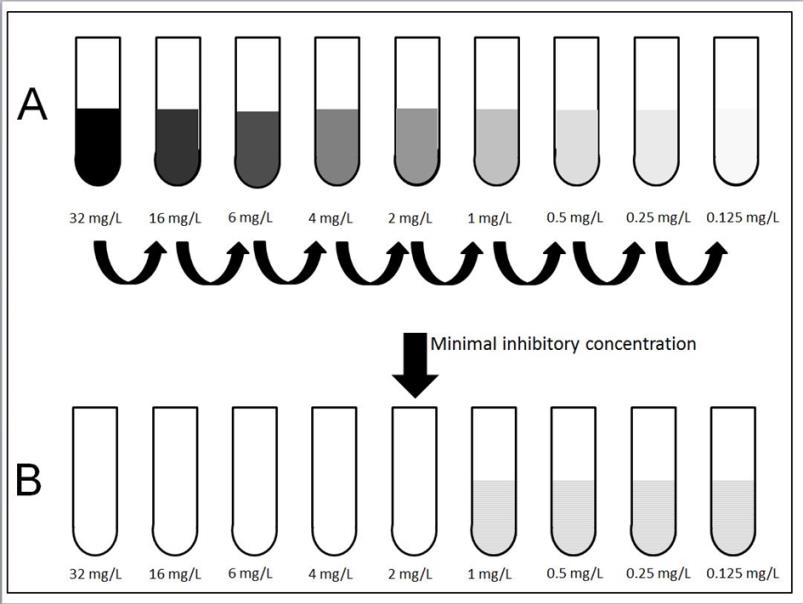
- a) Mikrodiffusionsverfahren

- b) Gradientendiffusion
Abb. 3: Induktionsphänomen bei der Disk-Diffusions-Methode
Nachweis des iMLS-Resistenzmechanismus (induzierbare Resistenz gegenüber Clindamycin)
Weiterführende Links
http://clsi.org/ast/
http://ecdc.europa.eu/en/healthtopics/antimicrobial_resistance/database/Pages/database.aspx
Referenzen
- Practical approach for reliable detection of AmpC beta-lactamase-producing Enterobacteriaceae.
Polsfuss S, Bloemberg GV, Giger J, Meyer V, Böttger EC, Hombach M (2011)
J Clin Microbiol. 49:2798-803. - Evaluation of a diagnostic flow chart for detection and confirmation of extended spectrum β-lactamases (ESBL) in Enterobacteriaceae.
Polsfuss S, Bloemberg GV, Giger J, Meyer V, Böttger EC, Hombach M (2012)
Clin Microbiol Infect. 18:1194-204. - Evaluation of the AID ESBL line probe assay for rapid detection of extended-spectrum β-lactamase (ESBL) and KPC carbapenemase genes in Enterobacteriaceae.
Bloemberg GV, Polsfuss S, Meyer V, Böttger EC Hombach M (2013)
J Antimicrob Chemother. 2013. 69:85-90. - Standardisation of disk diffusion results for antibiotic susceptibility testing using the sirscan automated zone reader.
Hombach M, Zbinden R, Böttger EC (2013)
BMC Microbiol. 13:225. - Validation of antibiotic susceptibility testing guidelines in a routine clinical microbiology laboratory exemplifies general key challenges in setting clinical breakpoints.
Hombach M, Courvalin P, Böttger EC (2014)
Antimicrob Agents Chemother. 58:3921-26. - Evaluation of carbapenemase screening and confirmation tests in Enterobacteriaceae and development of a practical diagnostic algorithm.
Maurer FP, Castelberg C, Quiblier C, Böttger EC, Bloemberg GV, Hombach M (2015)
J Clin Microbiol. 53:95-104.
Antimikrobielle Chemotherapie
Antibiotika-Richtlinien UniversitätsSpital Zürich
Im Auftrag des UniversitätsSpitals Zürich wurden Antibiotikarichtlinien erarbeitet, um den kostenbewussten Einsatz von Antibiotika im klinischen Alltag zu verbessern.
Diese werden von einer Arbeitsgruppe bestehend aus Mitarbeitern des UniversitätsSpitals Zürich und des IMM laufend aktualisiert.
Antibiotikarichtlinien 2014
Bitte richten Sie Ihre Bestellung per Email an: USZ


